
Cloruro de fosforilo
Acerca de este escuelas selección Wikipedia
Los artículos de esta selección escuelas se han organizado por tema currículo gracias a voluntarios SOS. Antes de decidir sobre el patrocinio de un niño, ¿por qué no aprender sobre diferentes obras de caridad de patrocinio primero ?
| Cloruro de fosforilo | |
|---|---|
 | |
 | |
Cloruro de fosforilo o | |
Otros nombres Oxicloruro de fósforo | |
| Identificadores | |
| CAS | 10025-87-3 |
| Número RTECS | TH4897000 |
| Propiedades | |
| Fórmula molecular | POCl3 |
| Masa molar | 153,33 g / mol |
| Apariencia | Claro, líquido incoloro, humos en el aire húmedo |
| Densidad | 1,645 g / cm 3, líquidos |
| Punto de fusion | 1.25 ° C (274,4 K) |
| Punto de ebullicion | 105.8 ° C (379,0 K) |
| Solubilidad en agua | Reacciona |
| Viscosidad | ? c P en? ° C |
| Estructura | |
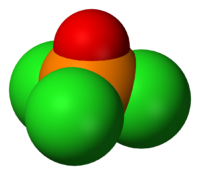
| Forma molecular | tetraédrica |
| Momento bipolar | 2.54 D |
| Peligros | |
| MSDS | MSDS externa |
| Frases R | 14-22-26-29-35-48 / 23 |
| Frases S | 26-45-7 / 8 |
| Principal peligros | Altamente corrosivo, lacrimógeno, tóxico |
| Compuestos relacionados | |
| Compuestos relacionados | Cloruro de tiofosforilo Fósforo oxibromuro |
| Página de datos complementaria | |
| Estructura y propiedades | n, ε r, etc. |
| Termodinámica datos | Comportamiento de fase Sólido, líquido, gas |
| Los datos espectrales | UV, IR, RMN , MS |
| Excepto cuando se indique lo contrario, los datos se den materiales en su condiciones normales (25 ° C, 100 kPa) | |
| Exenciones y referencias | |
Cloruro de fosforilo (comúnmente llamado oxicloruro de fósforo) es un líquido incoloro con la fórmula P O Cl 3. Se hidroliza en aire húmedo a ácido fosfórico para liberar vapores de asfixia cloruro de hidrógeno. Se fabrica industrialmente a gran escala a partir de tricloruro de fósforo y oxígeno o pentóxido de fósforo. Se utiliza principalmente para hacer ésteres de fosfato tales como fosfato de tricresilo.
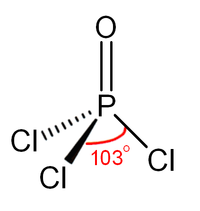
Estructura
Como fosfato, cloruro de fosforilo es tetraédrica en forma. Cuenta con tres enlaces P-Cl y un P muy fuerte = O doble enlace, con un estimado energía de disociación de enlace 533,5 kJ / mol. Sobre la base de longitud de enlace y electronegatividad, la regla Schomaker-Stevenson sugiere que la forma doble enlace es muy dominante (en contraste con POF 3). La P = enlace O no se parece al enlace π en una grupo carbonilo como en una cetona. La descripción adecuada de la interacción PO es un tema de largo debate. Los libros de texto de más edad que se convoque una descripción que invoca la participación de la d -orbitals en fósforo. Algunos de estos orbitales d proyecto hacia el átomo de O, con la superposición de p -orbitals en oxígeno. Textos más modernos parecen favorecer una descripción donde el PO π unión implica la sigma * componentes de los bonos P-Cl. Estas descripciones no tienen en cuenta el papel de los orbitales d.

- donde pm = picometros
Propiedades químicas
POCl3 reacciona con el agua y alcoholes para dar ácido fosfórico o ésteres de fosfato, respectivamente, por ejemplo
- O = PCl 3 + 3 H 2 O → O = P (OH) 3 + 3 HCl
Si el agua se sustituye por un alcohol , los ésteres de fosfato de trialquilo resultado. Tales reacciones se realizan a menudo en presencia de un aceptor de HCl tal como piridina o una amina . Si POCl3 se calienta con un exceso de una fenol ( ArOH) en presencia de una Catalizador ácido de Lewis tal como cloruro de magnesio se forma un éster de fosfato de triarilo, por ejemplo:
- 3 C 6 H 5 OH + O = PCl 3 → O = P (OC 6 H 5) 3 + 3 HCl
POCl3 también puede actuar como una Base de Lewis, formando aductos con una variedad de ácidos de Lewis tales como tetracloruro de titanio:
- Cl 3 P + -O - + TiCl4 → Cl 3 P + O- - TiCl4
El cloruro de aluminio aducto (POCl3 · AlCl 3) es bastante estable, y así POCl3 se puede utilizar para eliminar AlCl3 completamente a partir de mezclas de reacción al final de una Reacción de Friedel-Crafts. POCl3 reacciona con bromuro de hidrógeno en presencia de AlCl3 para producir POBr 3.
Preparación
Cloruro de fosforilo se puede preparar mediante la reacción de tricloruro de fósforo con oxígeno a 20-50 ° C (aire es ineficaz):
Una síntesis alternativa implica la reacción de pentacloruro de fósforo y pentóxido de fósforo. Dado que estos compuestos son sólidos, una manera conveniente de llevar a cabo la reacción es clorar una mezcla de PCl 3 y P 4 O 10, que genera el PCl5 in situ. Como se consume el PCl 3, el POCl3 se convierte en el disolvente de reacción.
6 PCl 5 + P 4 O 10 → 10 POCl3
Pentacloruro de fósforo también forma POCl3 por reacción con agua, pero esta reacción es menos fácil de controlar que la reacción anterior.
Usos
El uso más importante de cloruro de fosforilo es en la fabricación de ésteres de triarylphosphate (como se describe anteriormente ), tales como fosfato de trifenilo y fosfato de tricresilo. Estos ésteres se han utilizado durante muchos años como retardantes de llama y plastificantes para PVC. Mientras tanto ésteres de trialquilo tales como fosfato de tributilo (hecho de manera similar de butan-1-ol) se utilizan como disolventes de extracción líquido-líquido en reprocesamiento nuclear y en otros lugares.
En la industria de semiconductores, POCl3 se utiliza como una fuente de fósforo líquido seguro en procesos de difusión. El fósforo actúa como un dopante utilizado para crear capas de tipo N en una oblea de silicio.
En el laboratorio, POCl3 se utiliza ampliamente como un agente deshidratante, por ejemplo la conversión de amidas a nitrilos. Del mismo modo, ciertas amidas cíclicas pueden ciclarse en dihidrotestosterona derivados de isoquinolina utilizando el Reacción Bischler-Napieralski.
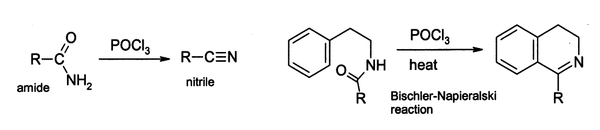
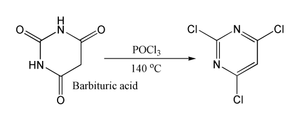
Tales reacciones se cree que ir a través de una cloruro de imidoilo; en ciertos casos en los que es estable, el cloruro de imidoilo es el producto final. Por ejemplo piridonas y pirimidonas se pueden convertir en derivados de cloro- piridinas y pirimidinas, que son intermedios importantes en la industria farmacéutica. Igualmente ácido barbitúrico se convierte en 2,4,6-tricloropirimidina. por reacción con POCl3 a 140 ° C.
Relacionado con esta química es el uso de POCl3 en acilación de activado anillos aromáticos a través de la Reacción para producir Vilsmeier-Haack arilo aldehídos y cetonas . La reacción más a menudo utiliza una formamida tal como DMF o N-fenil-N -methylformamide, y produce una sal de iminio que es fácilmente hidrolizado para dar el aldehído en estudio diagnóstico. Por ejemplo antraceno-9 da anthraldehyde:
